Cadmium (HU)
Traduction anglaise : Cadmium
Dernière mise à jour : 16/09/2022
Métal pauvre de numéro atomique 48 et de symbole Cd, aux propriétés proches de celles du zinc, souvent assimilé aux métaux de transition et présentant une toxicité et une écotoxicité importante, ce qui justifie son classement parmi les métaux lourds.
Sommaire |
Nature et différentes formes physico-chimiques
Le cadmium est présent naturellement à de très faibles concentrations dans la croûte terrestre et on le retrouve principalement dans les minerais de zinc. Il est également présent dans les minerais de plomb et de cuivre, ainsi que dans certains phosphates naturels.
Dans l'eau pure, le cadmium se trouve principalement sous la forme d'ions Cd2+, qui peuvent représenter jusqu'à 92% du cadmium total. Lorsque la teneur en sel augmente, on voit apparaître des chlorures (CdCl+, CdCl2, CdCl3-). Ces chlorures s'adsorbent moins facilement sur les particules que d'autres complexes à base de cadmium. La complexation du cadmium semble augmenter en présence d'effluents sanitaires urbains. On a ainsi observé dans certaines eaux que 51% du cadmium se trouvait sous la forme d'ions libres, 20% sous la forme de complexes humiques et 3,6% sous la forme CdOH+. Même lorsque le cadmium est présent dans la phase solide, il est essentiellement associé avec la fraction échangeable et donc très facilement remobilisable en cas de modification des conditions environnementales (pH, potentiel redox, salinité, etc.) (Ellis et al., 2004).
Sources et concentrations moyennes
Différentes sources de cadmium dans l'environnement
Les principales sources naturelles contribuant à diffuser le cadmium dans l'environnement sont les volcans, les incendies de forêts et les embruns océaniques. Ces sources naturelles semblent représenter la part principale des apports à l'échelle mondiale. Les apports anthropiques peuvent cependant être prépondérants localement.
Dans les sols des zones rurales les apports d'engrais phosphatés naturels ont constitué une source très importante dans les années 1970. Ces apports se sont cependant réduits, principalement parce que la consommation d'engrais phosphatés s'est réduite (en France par exemple, la consommation d’engrais phosphatés a été divisée par cinq entre 1978 et 2018). La réglementation a également progressivement limité la concentration autorisée en cadmium (par exemple 90 mg/kg de P2O5 en France). La réglementation a été homogénéisée au niveau européen en 2019 (data.consilium.europa.eu) et les engrais distribués en Europe sont plafonnés depuis 2022 à 60 mg/kg, avec comme objectif final d’atteindre 20 mg/kg d’ici dix ans
En ville, les sources industrielles sont beaucoup plus nombreuses. Le cadmium est utilisé dans les batteries (Nickel-Cadmium), pour protéger l'acier (cadmiage), dans un grand nombre de pigments, dans des agents stabilisants, dans les écrans de télévision, dans les cellules photovoltaïques, etc. La réglementation REACH impose depuis décembre 2011 une limitation plus stricte (voire une interdiction) de l'utilisation du cadmium dans la bijouterie, les plastiques, les peintures, les stabilisants et sur certains métaux. L'utilisation des batteries Ni-Cd a également été interdite à partir de 2017 par la directive 2006/66/CE du septembre 2006 pour les usages domestiques. Ces batteries sont cependant toujours utilisées pour les usages industriels (avec l'hypothèse que leur recyclage est plus facile dans ce cadre) et la fabrication de batteries Ni-Cd constitue de loin l'utilisation principale en Europe (figure 1).
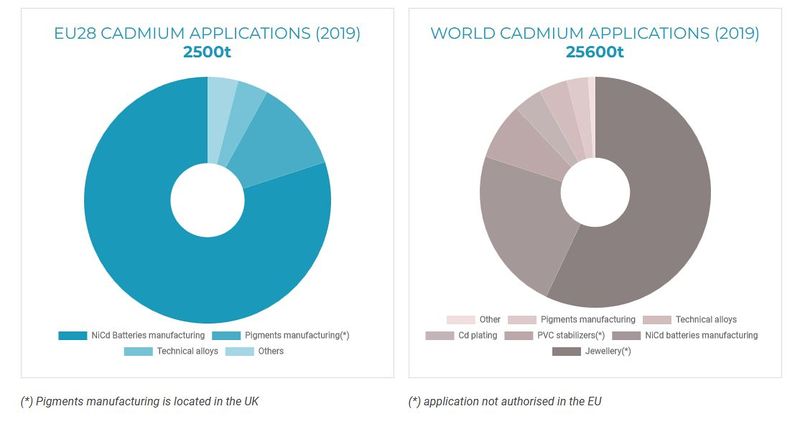
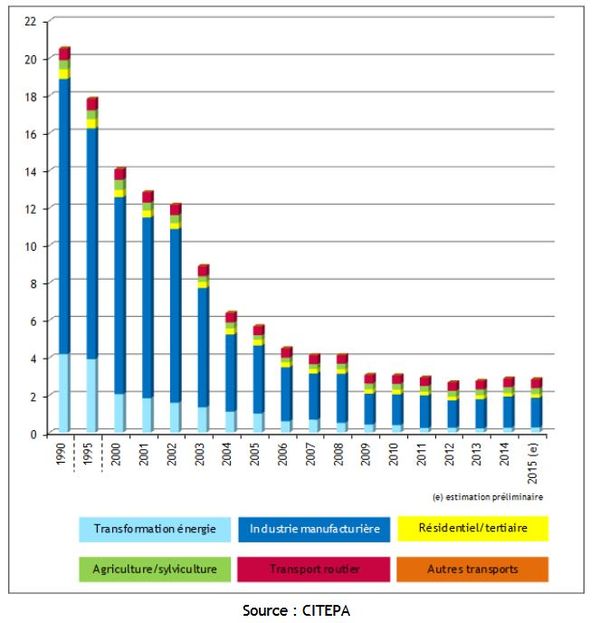
En 2019, 2 500 tonnes de cadmium ont été produites industriellement en Europe et 26 000 dans le monde (International cadmium association). Il est difficile de savoir exactement quelle part est rejetée dans l'environnement, mais on peut cependant observer que les efforts faits pour limiter les émissions et améliorer le recyclage ont été très efficaces jusqu'au début des années 2000 (figure 2 et 3) et ont permis de descendre aux niveaux les plus faibles depuis le début de l'ère industrielle (figure 2).
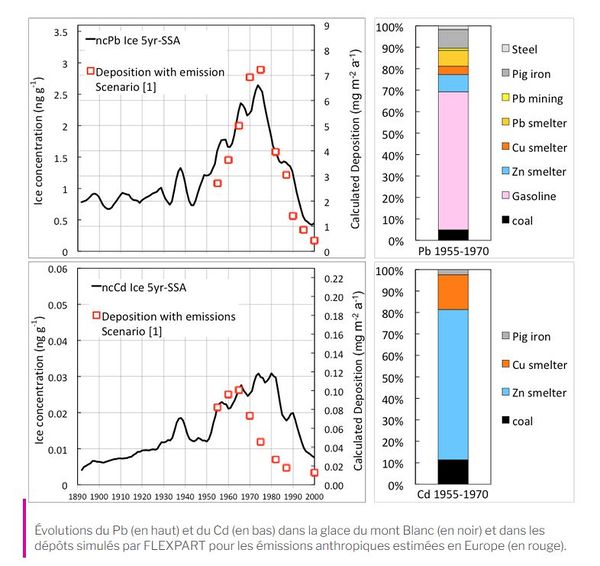
Cette diminution dans les émissions ne semble cependant plus se poursuivre actuellement dans les apports aux milieux aquatiques (avec cependant de grandes disparités), soit parce que les émissions ont cessé de diminuer, soit du fait du relargage de cadmium stocké depuis plus d'un siècle dans les sols et dans les sédiments (figure 4).
Contribution des rejets d'assainissement
Lors du projet AMPERE (Coquery et al, 2011 et http://projetamperes.cemagref.fr/), les concentrations en cadmium ont été mesurées à l'entrée et à la sortie de 21 stations d'épuration françaises. Les concentrations moyennes trouvées sont très variables mais se situent généralement entre 0,1 et 1 μg/L dans les eaux brutes en entrée et entre 0,01 et 0.1 μg/L dans les eaux traitées. La masse rejetée aux milieux aquatiques a été estimée en moyenne à 12 μg/j/hab, soit 0.8 tonne par an.
Comme l'évolution des émissions pouvait le laisser supposer, les concentrations moyennes événementielles observées pour le cadmium ont beaucoup baissé dans les eaux de ruissellement urbain au cours des dernières décennies. Alors que l'on pouvait atteindre jusqu'à 50 μg/L dans les années 1980 (Deutsch et al, 1982), les concentrations actuellement observées sont le plus souvent comprises entre 0,2 et 0,8 μg/L (Al-Juhaishi, 2018, Becouze-Lareure, 2010, Dembélé, 2010, Dutordoir, 2014, Gromaire, 2012, Moilleron, 2004, Zgheib, 2009), aussi bien dans les eaux pluviales que dans les eaux unitaires, soit du même ordre de grandeur que dans les eaux usées en entrée de station. Même si les volumes rejetés par temps de pluie sont beaucoup plus faibles que ceux rejetés par temps sec, la masse totale annuelle de cadmium due au rejets urbains de temps de pluie est probablement du même ordre de grandeur que celle rejetée par les stations d'épuration.
Dans les rejets urbains de temps sec comme de temps de pluie, plus de 80% du cadmium se trouve dans la phase dissoute et seule la fraction organique et la fraction échangeable se retrouve dans la phase solide. Pendant son transfert dans le réseau de transport, le cadmium a en effet tendance à s'associer avec des formes ioniques, faiblement complexées, et seul de 30 à 40% du cadmium est effectivement sous une forme très facilement biodisponible lors du rejet.
Les valeurs courantes de concentration ne posent pas de difficulté dans la mesure où la concentration maximum autorisée pour le cadmium et ses composés dans les rejets en provenance des installations classées pour la protection de l'environnement est de 25 μg/L.
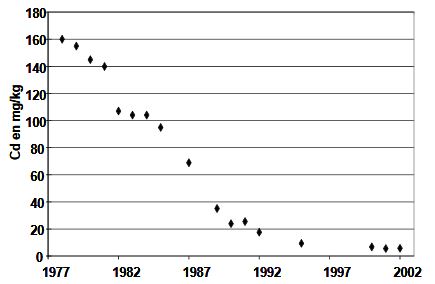
La concentration en cadmium dans les boues de station d'épuration constitue également un enjeu important pour leur valorisation agricole. Cette concentration a aussi beaucoup diminué au cours des dernières décennies du XXème siècle (voir Figure 5). Elle est maintenant le plus souvent comprise entre 1 mg/kg et 10 mg/kg, c'est à dire généralement très en dessous de la limite de référence pour l'utilisation agricole qui est fixée à 20 mg/kg de matière sèche, la valeur limite étant de 40 mg/kg en valeur limite. Rappelons à ce propos que la concentration maximum autorisée en Europe pour les engrais phosphatés est de 60 mg/kg.
Les systèmes d'assainissement ne constituent donc plus l'une des sources importantes d'apport en cadmium aux milieux aquatiques .
Toxicité et danger associés
Impacts possibles sur la santé
Le cadmium est très toxique pour l'homme, même à faible dose. Une exposition prolongée peut induire une atteinte rénale, une fragilité osseuse, des effets sur l’appareil respiratoire, des troubles de la reproduction ainsi qu’un risque accru de cancer. Le cadmium est aussi suspecté d’entrainer des effets sur le foie, le sang et le système immunitaire (www.cancer-environnement.fr). Un empoisonnement par du cadmium étudié au japon dans les années 50 (maladie de Itai-Itai) est connu pour avoir provoqué des lumbagos extrêmement violents et des troubles de la mobilité.
Cependant, même si le cadmium est susceptible de se bioaccumuler chez l'homme, les apports directs ou indirects liés à l'eau ne semble pas les plus importants. En France, la limite de concentration fixée pour les eaux destinées à la consommation humaine est de 5 μg/L (l'OMS recommande pour sa part de ne pas dépasser 3 μg/L). La plupart des eaux distribuées ont des concentrations très inférieures à cette valeur limite.
Impacts possibles sur les milieux aquatiques
Le cadmium est toxique à faibles doses pour de nombreuses espèces animales et végétales. Sa toxicité pour les poissons d'eau douce a été beaucoup étudiée. Elle dépend de la dureté de l'eau et de sa température. Elle est très forte aux stades juvéniles lorsque les espèces sont les plus vulnérables. Les données issues de tests de toxicité effectués sur des macroinvertèbrés suggèrent que ce sont les crustacés qui sont les espèces les plus sensibles.
Les Normes de qualité environnementales pour les eaux de surface sont ainsi très inférieures à celle prise en compte pour les eaux souterraines (qui est identique à celle des eaux destinées à la consommation humaine) (figure 6).

Bibliographie :
- Al-Juhaishi, M.R.D. (2018) : Caractérisation et impact de la pollution dans les rejets urbains par temps de pluie (RUTP) sur des bassins versants de l'agglomération Orléanaise ; Thèse de doctorat, Institut des Sciences de la terre d'Orléans, 210p.
- Baize, D., Courbe, C., Suc, O., Schwartz, C., Tercé, M., Bispo, A., Sterckman, T., Ciesielski, H. (2006) : Épandages de boues d’épuration urbaines sur des terres agricoles : impacts sur la composition en éléments en traces des sols et des grains de blé tendre ; Courrier de l’environnement de l’INRA n°53, décembre 2006 ; téléchargeable sur : https://hal.archives-ouvertes.fr/hal-01199208/file/C53Baize.pdf
- Becouze-Lareure, C. (2010) : Caractérisation et estimation des flux de substances prioritaires dans les rejets urbains par temps de pluie sur deux bassins versants expérimentaux. Thèse de doctorat, INSA-Lyon, laboratoire DEEP, 298 p.
- Coquery M., Pomiès M., Martin-Ruel S., Budzinski H., Miège C., Esperanza M., Soulier C., Choubert J.-M.(2011) : Mesurer les micropolluants dans les eaux brutes et traitées - Protocoles et résultats pour l'analyse des concentrations et des flux ; Techniques Sciences et Méthodes, 1/2 : 25-43 ; disponible sur : projetamperes.cemagref.fr
- Dembélé, A. (2010) : MES, DCO et polluants prioritaires des rejets urbains de temps de pluie : mesure et modélisation des flux événementiels, Thèse de doctorat, INSA Lyon, DEEP.
- Deutsch, J.C. et al. (1982) : Caractérisation de la pollution des eaux de ruissellement par temps de pluie, SHF - XVIIe Journées de l'Hydraulique, Nantes, septembre 1982(question Il, Rapport nO 1, 8 pages).
- Dutordoir, S. (2014) : Bilan des flux de métaux, carbone organique et nutriments contenus dans une rivière alpine : part des rejets urbains de l‘agglomération de Grenoble et apports amont (Isère et Drac).
- Ellis, B., Chocat, B., Fujita, S., Rauch, W., Marsalek, J. (2004) : Urban drainage, a multilingual glossary ; IWA publishing ; 512p.
- Gromaire, M.-C. (2012) : Contribution à l’étude des sources et flux de contaminants dans les eaux pluviales urbaines. Mémoire HDR, Université Paris Est, 107p.
- Legrand, M., McConnell, J. R., Lestel, L., Preunkert, S., Arienzo, M., Chellman, N. J., Stohl, A., and Eckhardt, S.(2020) : Cadmium pollution from zinc-smelters up to four-fold higher than expected in western Europe in the 1980s as revealed by alpine ice ; Geophysical Research Letters ; disponible sur : https://doi.org/10.1029/2020GL087537
- Moilleron, R. (2004) : Hydrocarbures et métaux en milieu urbain. Mémoire HDR, 79 p.
- Zgheib, S. (2009) : Flux et sources des polluants prioritaires dans les eaux urbaines en lien avec l’usage du territoire. Thèse de doctorat, LEESU, Université Paris-Est, 349 p.
Pour en savoir plus :
- Damy, P.C. (2011) : Synthèse des connaissances sur l’origine et la disponibilité du cadmium dans les eaux continentales - Synthèse documentaire ; ONEMA, Agences de l'Eau, OIEAU ; 39p. ; disponible sur www.oieau.fr.
- Bisson, M. (2011) : Le cadmium et ses dérivés ; INERIS - Données technico-économiques sur les substances chimiques en France ; 75p. ; disponible sur le portail substances chimiques de l'INERIS.
 S'abonner à un flux RSS
S'abonner à un flux RSS